
强生是全球最大的医药公司之一,近日发布了2019年第三季度业绩报告,销售额达207.29亿美元,其中制药业务销售额达108.77亿美元,免疫学和肿瘤学增长迅速。强生制药业务快速增长的背后是丰富的管线储备,尤其是免疫学和肿瘤学方面,有多个潜在年销售额数十亿美元级别的重磅管线药物,同时强生在流感、抑郁症等鲜有新药出现的领域也有一些突破。
本文就结合治疗效果、创新性以及市场价值等情况盘点了截止2019年前三季度强生的10大药物。
TOP10 Apalutamide
Apalutamide 是一种非甾体类选择竞争性雄激素受体抑制剂,由强生在2013年以最高价格10亿美元收购Aragon时获得,于2018年2月获美国FDA批准治疗用于非转移性去势抵抗性前列腺癌。
Apalutamide是Aragon的旗帜性药物,强生收购Aragon主要是看重了Apalutamide,想保持住其在前列腺癌药物领域的优势地位。
目前最畅销的药物阿比特龙面临专利到期的问题,Apalutamide可以作为一个有力的补充。目前Apalutamide还有多个临床研究正在进行中,其中包括中国地区,这无疑对中国患者来说是个好消息。同样机制的Xtandi其价格高达每疗程12.9万美元,而且在国内还没有上市。
TOP9 Pimodivir
Pimodivir是一种治疗流感的药物,其靶点是流感病毒聚合酶复合物pb2 亚单位,是first-in-class药物。强生在2014年从位于波士顿的生物制药公司vertex pharmaceuticals那里获得了Pimodivir的全球开发权益。
甲型流感治疗的关键在于如何克服耐药性,而Pimodivir可以抑制流感病毒聚合酶复合物pb2亚单位,很好的解决了耐药性这一问题。该药已经于2017年6月完成了用于季节性甲型流感成人患者治疗的临床IIb期研究,试验结果比较积极:相对比安慰剂组,Pimodivir单药用药可以显著降低病患的病毒载量达7天之久,与此同时,Pimodivir与Oseltamivir联用可以将病患的病毒载量降到更低水平,且无严重的不良反应。
Pimodivir已经在2017年3月获得了美国FDA的快速通道地位,于2017年下半年开始临床III期研究,预计2020年能够上市。
TOP8 Guselkumab
Guselkumab用于治疗中度至重度的板块性银屑病,于2017年7月13日获美国FDA批准上市,是全球第一个抗IL-23单抗药物。强生发布的临床研究结果表明,不同剂量下Guselkumab治疗斑块性银屑病的效果显著优于修美乐(阿达木单抗),单凭在这一点还不足以说明此药将会成为重磅炸弹式药物,强生还在积极扩大此药的适应症范围,目前用于治疗银屑病性关节炎、克罗恩病、小儿银屑病等多种自身免疫疾病的临床研究正在进行中。
Guselkumab自上市以来表现不错,2019年前三季度销售额达7.42亿美元。
TOP7 Erdafitinib
Erdafitinib 是FDA批准的首款成纤维细胞生长因子受体(FGFR)激酶抑制剂,于2019年4月获美国FDA加速批准,用于治疗携带易感FGFR3或FGFR2基因改变、并且接受至少一种含铂化疗期间或之后病情进展的局部晚期或转移性膀胱上皮癌成人患者。Erdafitinib由Astex制药公司发现,强生在2008年与Astex达成独家全球授权和合作协议,共同开发和商业化Erdafitinib。目前,Erdafitinib还有多个临床研究正在进行中,业界人士很看好此药的销售前景,预计年销售额将不低于10亿美元。
TOP6 Esketamine
不同于已上市抗抑郁药物,Esketamine这种新型抗抑郁药物是一种非竞争性的N-甲基-D天冬氨酸受体拮抗剂,通过调节谷氨酸受体活性调节抵抗性抑郁症患者大脑细胞之间的神经突触的可塑性,从而迅速并且持久地改善患者症状,同时它还具有多巴胺再摄取抑制剂的功能。
2018年9月杨森向美国FDA递交Esketamine鼻喷雾剂的新药上市申请,用于治疗成年治疗抵抗性抑郁症患者,2019年3月被FDA批准。Esketamine成为近50年来治疗难治性严重抑郁症的首个新药。2018年10月在欧盟提交了新药上市申请,预计获批在即。该药针对伴有自杀风险重度抑郁症的III期临床研究也在进行中,据统计全球有接近3亿严重抑郁症患者,其中三分之一的患者对现有疗法没有反应,急需多种新药来帮助病人摆脱这种精神疾病的困扰,因此Esketamine的潜在市场非常巨大。
TOP5 Niraparib
Niraparib是一种口服高特异性多聚腺苷二磷酸核糖聚合酶(PARP)抑制剂,通过抑制PARP来扰乱PARP介导的DNA损伤修复通路。在携带BRCA1/2基因突变或者DNA重组修复机制缺失的肿瘤细胞中,PARP抑制剂会导致过多的DNA损伤无法修复,从而杀死肿瘤细胞。
Niraparib最初由TESARO公司开发,目前已经获得批准治疗卵巢癌。强生旗下的杨森制药在2016年与TESARO公司达成协议,买下了Niraparib前列腺癌的全球开发权利,仅是这一个适应症就花了强生0.35亿美元的预付款、4.5亿美元的里程金,另外还有一定的销售分红。目前该药处于转移性去势抵抗性前列腺癌患者的II期临床研究,2019年2月强生在ASCO GU会议上公布了初步结果:Niraparib治疗携带BRCA1/2基因突变的去势抵抗前列腺癌患者的客观缓解率约40%。强生在前列腺癌药物方面经验丰富,它的Zytiga(阿比特龙)2019年上半年销售额高达13.77亿美元,是全球销售额最高的前列腺癌药物,强生购入Niraparib的前列腺癌开发权利可谓是强强联手,此药的前景比较乐观。
TOP4 JNJ-68284528
JNJ-68284528又名LCARB-38M,由强生与南京传奇联合开发,目前处于2期临床研究阶段。2019年5月获得欧洲药品管理局(EMA)授予的PRIME认证,用于治疗晚期复发或难治性多发性骨髓瘤。JNJ-68284528是一种以B细胞成熟抗原(BCMA)为靶点的CAR-T疗法。BCMA是一种跨膜糖蛋白,属于肿瘤坏死因子(TNF)受体超家族,广泛存在于多发性骨髓瘤(MM)细胞表面。CAR- T疗法可以特异性地识别肿瘤相关抗原,使效应T细胞的靶向性、杀伤活性和持久性均高于常规应用的免疫细胞,并可克服肿瘤局部免疫抑制微环境并打破宿主免疫耐受状态。JNJ-68284528作为这种热门靶点和热门方法结合的药物其临床效果和上市前景都值得令人期待。
TOP3 Ponesimod
Ponesimod是一种选择性鞘氨醇-1-磷酸受体1(S1P1)调节剂,用于治疗治疗复发型多发性硬化病(RMS)。该药物能够功能性抑制S1P活性并将淋巴细胞束缚在淋巴结内,从而减少循环淋巴细胞的数量,防止炎性免疫细胞越过血脑屏障进入中枢神经系统(CNS)和损害髓鞘。
此药目前正处于临床III期研究阶段,2019年09月强生首次对外发布了Ponesimod治疗复发型多发性硬化症成人患者的头对头III期研究OPTIMUM结果,该研究比较了Ponesimod与Aubagio的疗效、安全性和耐受性。Aubagio是目前一款处于行业领先位置口服MS药物,在全球超过70个国家上市,年销售额超过10亿美元。临床试验结果显示,Ponesimod在研究的主要终点和多个次要终点方面均显示出优越性,同时Ponesimod具有良好的安全性和耐受性,这都证明Ponesimod是非常具有潜力的新型治疗多发性硬化病的药物,预计强生明年将会把此药推向市场,不过它将会遇到不小的竞争压力。
今年3月,同为S1P-1调节剂的Mayzent(诺华)获美国FDA批准上市,此外,今年6月,来自新基的口服S1P受体调节剂Ozanimod治疗RMS的监管申请文件获美国FDA和欧盟EMA受理。Ponesimod是否能够后来居上有待进一步观察。
TOP2 Ibrutinib
Ibrutinib是一种不可逆布鲁顿酪氨酸激酶(BTK)抑制剂,此药为强生和艾伯维共有,其中强生负责美国以外的销售。此药的最早由美国制药公司Celera Genomics开发,他们通过以化学结构为基础的途径合成了一系列小分子物质,这些小分子通过与ATP结合域附近的半胱氨酸-481共价结合灭活BTK,同时还可以与半胱氨酸靶向结合的方式不可逆地抑制BTK。2006年Pharmacyclics从Celera Genomics把Ibrutinib收购,随后强生公司制药事业部参与合作,与Pharmacyclics公司一起开发,将其用于多种B细胞恶性肿瘤。
2013年11月美国FDA批准ibrutinib用于治疗套细胞淋巴瘤,是首个获批BTK抑制剂。截止目前Ibrutinib被批准上市的适应症已经多达7种。此药还有很大的可挖潜力,潜在适应症包括了多种淋巴瘤如非霍奇金淋巴瘤、弥散性大B细胞淋巴瘤、边缘性淋巴瘤以及一线治疗慢性淋巴瘤系白血病,目前有数十个个III期临床研究正在进行当中。
此药2019年前三季度销售额已经超过了25.36亿美元,随着临床研究的推进以及新的适应症获批,其销售额还将大幅上涨。
TOP1 Darzal
Darzalex于2015年11月被FDA批准用于接受过至少3种治疗方案的多发性骨髓瘤患者,成为全球首个上市的针对肿瘤浆细胞表面的CD38分子的单克隆抗体,可以通过包括补体依赖性细胞毒作用、抗体依赖性细胞介导的细胞毒作用和抗体依赖性细胞吞噬作用等多种免疫介导的作用机制诱导肿瘤细胞的快速死亡,不仅如此,Daratumumab的也够靶向免疫抑制细胞来提高肿瘤微环境中的免疫性。
Darzalex自2015年上市以来,已经在多发性骨髓瘤治疗领域斩获了多项适应症,从最初的四线疗法扩大到一线疗法,最近的消息是2019年9月26日,强生向FDA提交了Darzalex联合标准护理(硼替佐米+沙利度胺+低剂量地塞米松,VTd)一线治疗适合自体干细胞移植(ASCT)的多发性骨髓瘤患者的补充生物制品许可申请。若顺利通过,将更加巩固Darzalex一线治疗多发性骨髓瘤的地位。由于CD38在多种肿瘤细胞中高表达,除了多发性骨髓瘤外,Daratumumab的潜在适应症包括多种血液肿瘤、淋巴瘤,以及非小细胞肺癌、胰腺癌、结直肠癌、乳腺癌、头颈癌等多种实体瘤,目前有多个临床研究正在进行中。
Darzalex 2019年前三季度的销售额已经达到了21.68亿美元,随着其适应症范围不断扩大,销售额肯定也会水涨船高,多发性骨髓瘤的市场容量很大,仅来那度胺的销售额一年就将近100亿美元,再加上Darzalex还很有可能涉及到其他肿瘤治疗领域,其峰值年销售额非常有机会突破100亿美元。
表1. 强生10大潜力药物一览
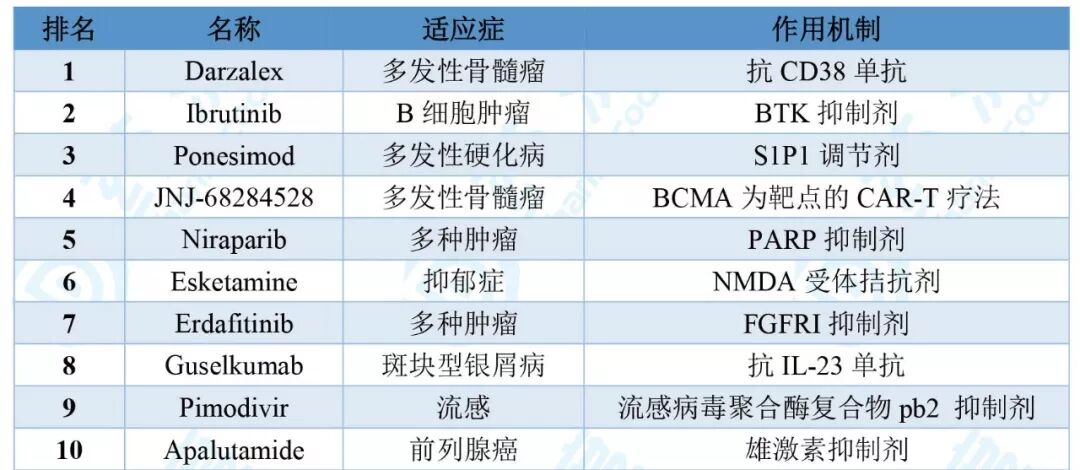
主要参考资料:1. 药渡数据库2. 强生官网3. FDA官网



上周热门文章精选
《信立泰注射用特立帕肽上市申请获批 国内骨质疏松市场或将再起波澜》
《一文读懂免疫治疗之超进展》
《国内Biotech研发管线系列 | 君实生物:一超多强,积极拓展PD-1适应症》
《Pfizer公布特应性皮炎新药Abrocitinib详细III期临床数据,挑战Dupixent!》
《诺诚健华赴港IPO,成立不到4年,估值8.8亿,奥布替尼与赞布替尼撞款》
《罗氏晒出Q1-Q3业绩:461亿CHF、制药业务+12%、多项里程碑进展》
《仑伐替尼成大热门 4家争夺首仿!与K药联用一线治疗多个癌症进入Ⅲ期》
来源:药渡网
声明:本文仅代表作者观点,并不代表制药在线立场。本网站内容仅出于传递更多信息之目的。如需转载,请务必注明文章来源和作者。
客服热线:400 610 1188
投稿邮箱:Kelly.Xiao@imsinoexpo.com
▼更多精彩推荐,请关注我们▼

把时间交给阅读
